Lựa chọn câu để xem lời giải nhanh hơn
CH tr 26 MĐ
|
Trong nguyên tử, các electron chuyển động như thế nào và chiếm những mức năng lượng nào? Trình tự sắp xếp các mức năng lượng này ra sao? Việc phân bố các electron trong nguyên tử tuân theo những nguyên lí và quy tắc nào?
|
Lời giải chi tiết:
– Theo mô hình hiện đại, các electron chuyển động rất nhanh xung quanh hạt nhân không theo một quỹ đạo xác định, tạo thành đám mây electron
– Các electron được sắp xếp thành từng lớp và phân lớp theo năng lượng từ thấp đến cao
– Trình tự sắp xếp các mức năng lượng:
+ Các electron trên cùng một phân lớp có năng lượng bằng nhau
+ Các electron trên cùng một lớp có năng lượng gần bằng nhau
CH tr 26 CH
|
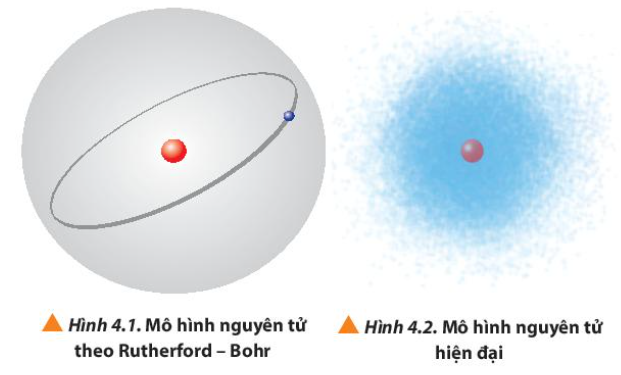
1. Quan sát Hình 4.1 và 4.2, so sánh điểm giống nhau và khác nhau giữa mô hình Rutherford – Bohr với mô hình hiện đại mô tả sự chuyển động của electron trong nguyên tử
|
Phương pháp giải:
Quan sát Hình 4.1 và 4.2 => So sánh
Lời giải chi tiết:
|
|
Hình 4.1
|
Hình 4.2
|
|
Giống nhau
|
Chuyển động xung quanh hạt nhân
|
|
Khác nhau
|
Quỹ đạo hình tròn hoặc bầu dục xác định xung quanh hạt nhân
|
Chuyển động rất nhanh xung quanh hạt nhân, không theo quỹ đạo xác định
|
CH tr 27 VD
|
Hệ Mặt Trời gồm Mặt Trời ở trung tâm và các thiên thể quay quanh theo những quỹ đạo xác định. Hãy cho biết mô hình nguyên tử của nhà khoa học nào được gọi là mô hình hành tinh nguyên tử, tương tự như hệ Mặt Trời?

|
Phương pháp giải:
– Theo Rutherford – Bohr: các electron chuyển động trên những quỹ đạo hình tròn hay bầu dục xác định xung quanh hạt nhân
– Theo mô hình hiện đại: chuyển động rất nhanh xung quanh hạt nhân, không theo một quỹ đạo xác định
Lời giải chi tiết:
– Các thiên thể quay quanh Mặt Trời theo quỹ đạo xác định
– Theo Rutherford – Bohr: các electron chuyển động trên những quỹ đạo hình tròn hay bầu dục xác định xung quanh hạt nhân
=> Mô hình nguyên tử của Rutherford – Bohr được gọi là mô hình hành tinh nguyên tử, tương tự như hệ Mặt Trời
CH tr 27 CH
|
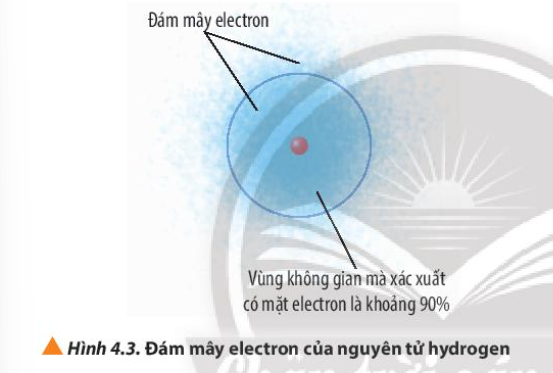
2. Quan sát Hình 4.3, phân biệt khái niệm đám mây electron và khái niệm orbital nguyên tử
|
Phương pháp giải:
– Đám mây electron: khu vực không gian xung quanh hạt nhân mà có electron
– Orbital nguyên tử: khu vực không gian xung quanh hạt nhân mà xác suất có mặt electron khoảng 90%
Lời giải chi tiết:
– Đám mây electron là khu vực có sự có mặt của electron xung quanh hạt nhân
– Orbital nguyên tử là khu vực mà xác suất có mặt electron là 90% xung quanh hạt nhân
CH tr 27 CH
|
3. Cho biết khái niệm orbital nguyên tử xuất phát từ mô hình nguyên tử của Rutherford – Bohr hay mô hình nguyên tử hiện đại
|
Phương pháp giải:
Orbital nguyên tử là khu vực không gian xung quanh hạt nhân mà tại đó xác suất có mặt (xác suất tìm thấy) electron khoảng 90%
Lời giải chi tiết:
Orbital nguyên tử là khu vực không gian xung quanh hạt nhân mà tại đó xác suất có mặt (xác suất tìm thấy) electron khoảng 90%
=> Xuất phát từ mô hình nguyên tử hiện đại vì electron chuyển động không theo quỹ đạo, mật độ electron không giống nhau
CH tr 27 CH
|
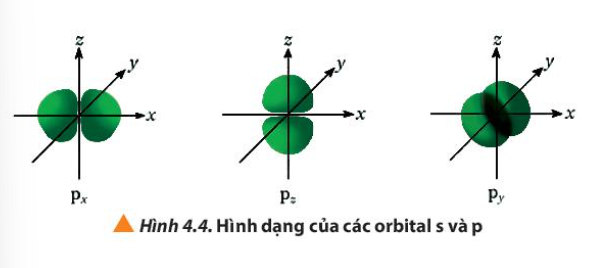
4. Quan sát Hình 4.4, hãy cho biết điểm giống và khác nhau giữa các orbital p (px, py, pz)
|
Phương pháp giải:
Quan sát Hình 4.4 và so sánh
Lời giải chi tiết:
|
|
px
|
py
|
pz
|
|
Giống nhau
|
Đều có hình dạng là số 8 nổi
|
|
Khác nhau
|
Nằm trên trục Ox
|
Nằm trên trục Oy
|
Nằm trên trục Oz
|
CH tr 28 CH
|
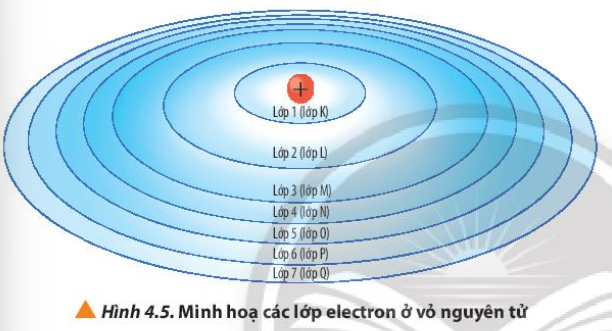
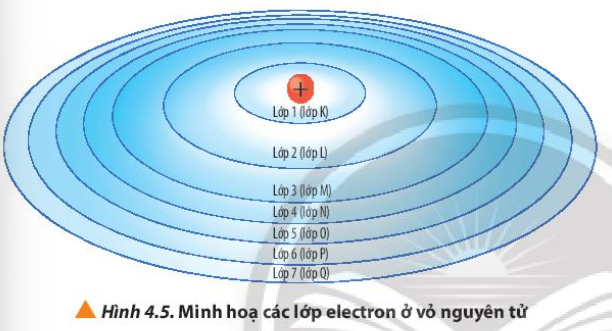
5. Quan sát Hình 4.5, nhận xét cách gọi tên các lớp electron bằng các chữ cái tương ứng với các lớp từ 1 đến 7
|
Phương pháp giải:
Quan sát Hình 4.5 và gọi tên
Lời giải chi tiết:
– Lớp 1 – Lớp K
– Lớp 2 – Lớp L
– Lớp 3 – Lớp M
– Lớp 4 – Lớp N
– Lớp 5 – Lớp O
– Lớp 6 – Lớp P
– Lớp 7 – Lớp Q
=> Cách gọi tên theo bảng chữ cái từ K đến Q lần lượt ứng với các lớp từ 1 đến 7
CH tr 28 CH
|
6. Từ Hình 4.5, cho biết lực hút của hạt nhân với electron ở lớp nào là lớn nhất và lớp nào là nhỏ nhất
|
Phương pháp giải:
Các lớp càng gần hạt nhân thì lực hút càng lớn
Lời giải chi tiết:
– Lớp K gần hạt nhân nhất => Lực hút của hạt nhân với electron ở lớp K là lớn nhất
– Lớp Q nằm xa hạt nhân nhất => Lực hút của hạt nhân với electron ở lớp Q là nhỏ nhất
CH tr 28 CH
|
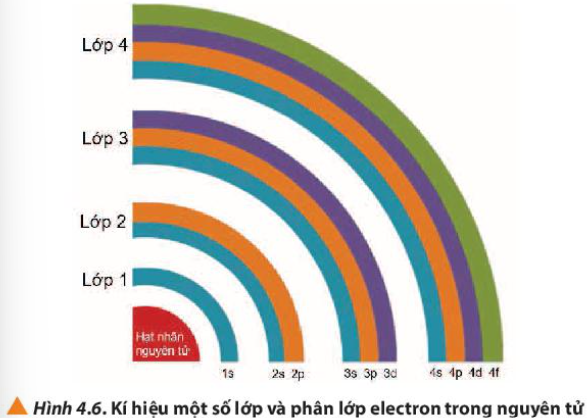
7. Quan sát Hình 4.6, nhận xét về số lượng phân lớp trong các các lớp từ 1 đến 4
|
Phương pháp giải:
Đếm số phân lớp => So sánh với số lớp
Lời giải chi tiết:
– Lớp 1 có 1 phân lớp
– Lớp 2 có 2 phân lớp
– Lớp 3 có 3 phân lớp
– Lớp 4 có 4 phân lớp
=> Từ lớp 1 đến lớp 4, số phân lớp trong mỗi lớp bằng số thứ tự của lớp đó
CH tr 29 CH
|
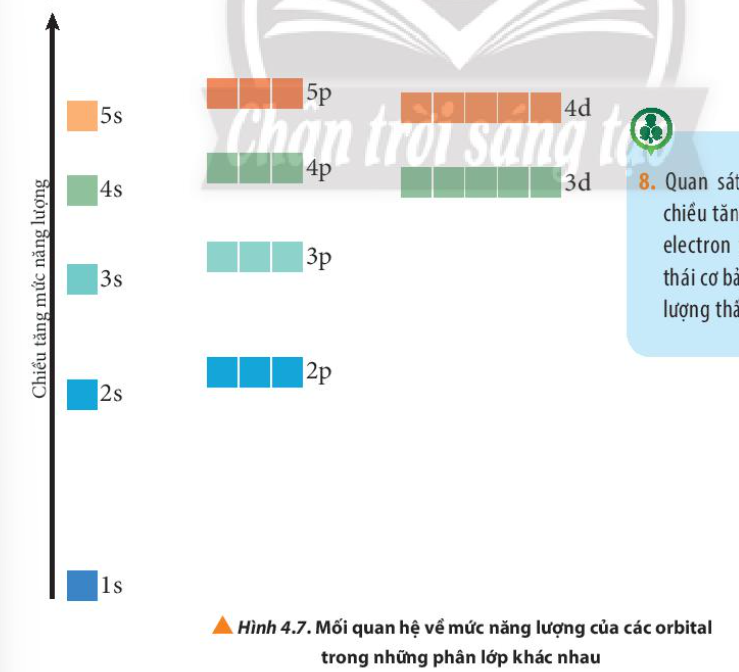
8. Quan sát Hình 4.7, nhận xét chiều tăng năng lượng của các electron trên các AO ở trạng thái cơ bản (trạng thái có năng lượng thấp nhất)
|
Phương pháp giải:
Quan sát Hình 4.7 và rút ra nhận xét
Lời giải chi tiết:
Ở trạng thái cơ bản, các electron trong nguyên tử chiếm lần lượt những orbital có mức năng lượng từ thấp đến cao: 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p…
CH tr 30 CH
|
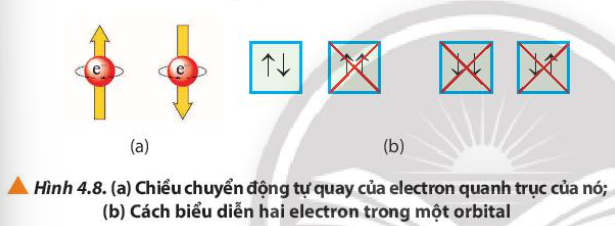
9. Quan sát Hình 4.8, cho biết cách biểu diễn 2 electron trong một orbital dựa trên cơ sở nào
|
Phương pháp giải:
Quan sát Hình 4.8 và rút ra nhận xét
Lời giải chi tiết:
Trong 1 orbital chỉ chứa tối đa 2 electron và có chiều tự quay ngược nhau
CH tr 30 CH
|
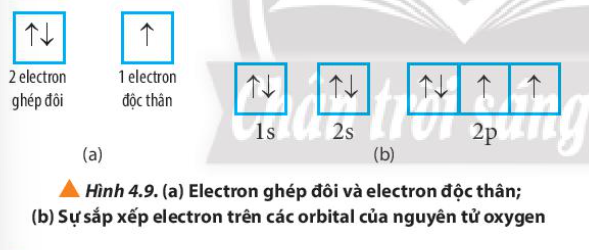
10. Quan sát Hình 4.9, hãy cho biết nguyên tử oxygen có bao nhiêu electron ghép đôi và bao nhiêu electron độc thân
|
Phương pháp giải:
Quan sát Hình 4.9 và rút ra nhận xét
Lời giải chi tiết:
– Nguyên tử oxygen có:
+ 6 electron ghép đôi nằm ở orbital 1s, 2s và 1 orbital 2p
+ 2 electron độc thân nằm ở 2 orbital 2p
CH tr 31 CH
|
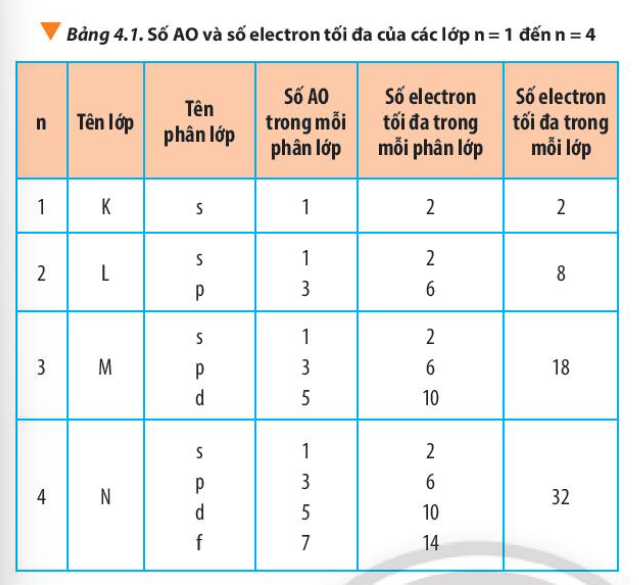
11. Từ Bảng 4.1, hãy chỉ ra mối quan hệ giữa số thứ tự lớp và số electron tối đa trong mỗi lớp
|
Phương pháp giải:
Quan sát Bảng 4.1 và rút ra nhận xét
Lời giải chi tiết:
– Lớp 1 có tối đa 2 electron = 2.12
– Lớp 2 có tối đa 8 electron = 2.22
– Lớp 3 có tối đa 18 electron = 2.32
– Lớp 4 có tối đa 32 electron = 2.42
=> Số electron tối đa trong lớp n là 2n2
CH tr 31 LT
|
Nguyên tử nitrogen có 2 lớp electron trong đó có 2 phân lớp s và 1 phân lớp p. Các phân lớp s đều chứa số electron tối đa, còn phân lớp p chỉ chứa một nửa số electron tối đa. Nguyên tử nitrogen có bao nhiêu electron?
|
Phương pháp giải:
Nitrogen có 2 lớp
– Lớp 1 có phân lớp 1s
– Lớp 2 có phân lớp 2s 2p
– Phân lớp s có tối đa 2 electron
– Phân lớp p có tối đa 6 electron
Lời giải chi tiết:
Nitrogen có 2 lớp
– Lớp 1 có phân lớp 1s
– Lớp 2 có phân lớp 2s 2p
– Phân lớp s có tối đa số electron => 1s có 2 electron, 2s có 2 electron
– Phân lớp p chỉ chứa 1 nửa số electron tối đa => 2p có 3 electron
=> Nguyên tử nitrogen có số electron = 2 + 2 + 3 = 7 electron
CH tr 31 CH
|
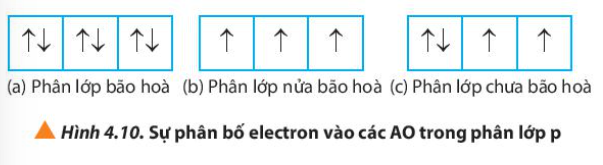
12. Quan sát Hình 4.10, hãy nhận xét số lượng electron độc thân ở mỗi trường hợp
|
Phương pháp giải:
Quan sát Hình 4.10 và rút ra nhận xét
Lời giải chi tiết:
(a) Phân lớp bão hòa => Không có electron độc thân
(b) Phân lớp nửa bão hòa => Số electron độc thân = số orbital của phân lớp đó
(c) Phân lớp chưa bão hòa => số electron độc thân nhỏ hơn số orbital trong phân lớp đó
CH tr 31 CH
|
13. Hãy đề nghị cách phân bố electron vào các orbital để số electron độc thân là tối đa
|
CH tr 31 LT
|
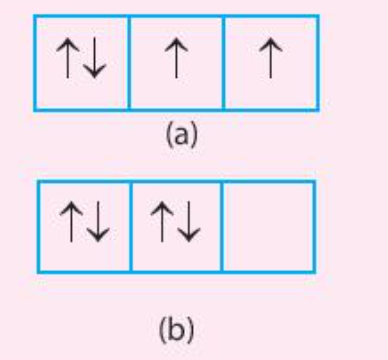
Trong các trường hợp (a) và (b) dưới đây, trường hợp nào có sự phân bố electron vào các orbital tuân theo và không tuân theo quy tắc Hund
|
Phương pháp giải:
Trong cùng một phân lớp chưa bão hòa, các electron sẽ phân bố vào các orbital sao cho số electron độc thân là tối đa
Lời giải chi tiết:
Cả 2 trường hợp (a) và (b) đều chưa đạt được phân lớp bão hòa
– Trường hợp (a) có 2 electron độc thân => Số electron độc thân đã tối đa
– Trường hợp (b) không có electron độc thân => Số electron độc thân chưa tối đa
=> Trường hợp (a) tuân theo quy tắc Hund, trường hợp (b) không tuân theo quy tắc Hund
CH tr 32 CH
|
14. Cấu hình electron của một nguyên tử cho biết những thông tin gì?
|
Phương pháp giải:
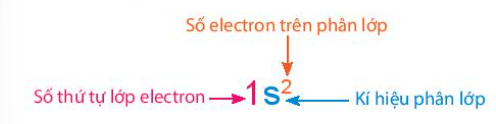
Lời giải chi tiết:
Cấu hình electron cho biết: số electron trên phân lớp, số electron lớp ngoài cùng, số lớp electron của nguyên tử
CH tr 32 LT
|
Viết cấu hình electron nguyên tử của nguyên tố aluminium (Z = 13) và biểu diễn cấu hình electron của aluminium theo ô orbital. Từ đó, xác định số electron độc thân của nguyên tử này.
|
Phương pháp giải:
Bước 1: Xác định số electron: 13
Bước 2: Viết thứ tự các lớp và phân lớp electron theo chiều tăng dần của năng lượng:
1s 2s 2p 3s 3p 4s 3d 4p
Bước 3: Điền các electron vào các phân lớp theo nguyên lí vững bền cho đến electron cuối cùng
Lời giải chi tiết:
– Nguyên tử có Z = 13 => Có 13 electron
– Viết theo thứ tự: 1s 2s 2p 3s 3p 4s 3d… (trong đó phân lớp s chứa tối ta 2 electron, phân lớp p chứa tối đa 6 electron, phân lớp d chứa tối đa 10 electron, phân lớp f chứa tối đa 14 electron)
– Điền các electron: 1s22s22p63s23p1
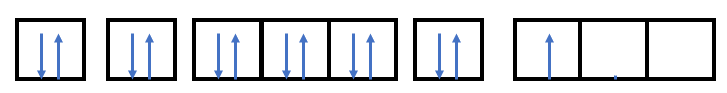
=> Nguyên tử aluminium có 1 electron độc thân
CH tr 33 CH
|
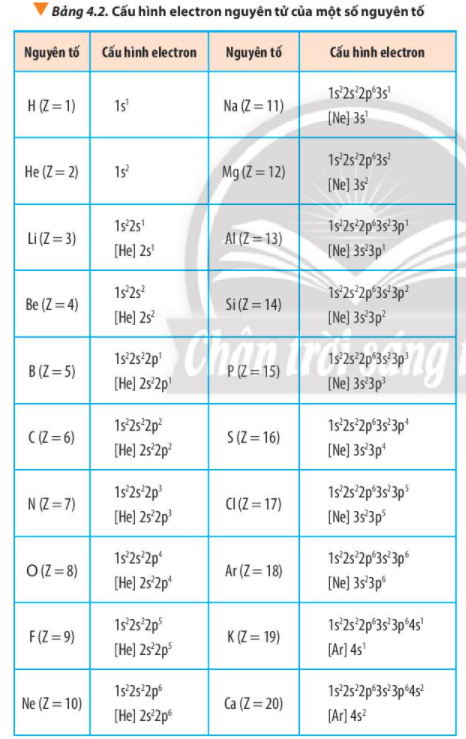
15. Quan sát Bảng 4.2, hãy cho biết dựa trên cơ sở nào để dự đoán phosphorus là nguyên tố phi kim
|
Phương pháp giải:
– Các nguyên tử có 1, 2, 3 electron ở lớp ngoài cùng là các nguyên tử của nguyên tố kim loại
– Các nguyên tử có 5, 6, 7 electron ở lớp ngoài cùng thường là nguyên tử của các nguyên tố phi kim
Lời giải chi tiết:
Theo Bảng 4.2 phosphorus có 5 electron ở lớp ngoài cùng
=> Phosphorus là nguyên tố phi kim
CH tr 33 VD
|
Lithium là một nguyên tố có nhiều công dụng, được sử dụng trong chế tạo máy bay và trong một số loại pin nhất định. Pin Lithium -lon (pin Li-lon) đang ngày càng phổ biến, nó cung cấp năng lượng cho cuộc sống của hàng triệu người mỗi ngày thông qua các thiết bị như máy tính xách tay, điện thoại di động, xe Hybrid, xe điện,… nhờ trọng lượng nhẹ, cung cấp năng lượng cao và khả năng sạc lại. Dựa vào cấu hình electron nguyên tử (Bảng 4.2), hãy dự đoán lithium là kim loại, phi kim hay khí hiếm?
|
Phương pháp giải:
– Các nguyên tử có 1, 2, 3 electron ở lớp ngoài cùng là các nguyên tử của nguyên tố kim loại
– Các nguyên tử có 5, 6, 7 electron ở lớp ngoài cùng thường là nguyên tử của các nguyên tố phi kim
– Các nguyên tử có 4 electron ở lớp ngoài cùng có thể là nguyên tử của nguyên tố kim loại hoặc phi kim
– Nguyên tử có 8 electron ở lớp ngoài cùng là nguyên tử của nguyên tố khí hiếm
Lời giải chi tiết:
Theo Bảng 4.2 lithium có 1 electron ở lớp ngoài cùng
=> Lithium là nguyên tố kim loại
Bài tập 1
|
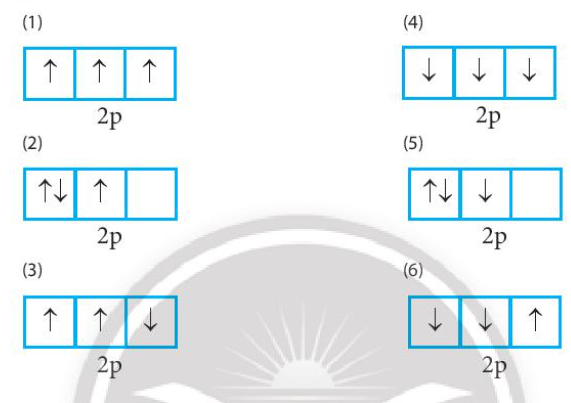
Bài 1: Trong các cách biểu diễn electron và các orbital của phân lớp 2p ở trạng thái cơ bản, hãy chọn cách phân bố đúng:
|
Phương pháp giải:
– Trong cùng một phân lớp chưa bão hòa, các electron sẽ phân bố vào các orbital sao cho số electron độc thân là tối đa
– AO chứa electron độc thân: ↑
– AO chứa electron ghép đôi: ↑↓
Lời giải chi tiết:
(1): đúng vì chứa tối đa electron và biểu diễn electron độc thân bằng mũi tên đi lên
(2): sai vì số electron độc thân chưa tối đa
(3): sai vì biểu diễn 1 electron độc thân bằng mũi tên đi xuống
(4): sai vì biểu diễn electron độc thân bằng mũi tên đi xuống
(5): sai vì số electron độc thân chưa tối đa, biểu diễn electron độc thân bằng mũi tên đi xuống
(6): sai vì biểu diễn 2 electron độc thân bằng mũi tên đi xuống
Bài tập 2
|
Bài 2: Cho nguyên tố X có 2 lớp electron, lớp thứ 2 có 6 electron. Xác định số hiệu nguyên tử của X
|
Phương pháp giải:
– Lớp thứ nhất: có 1 phân lớp là 1s
– Lớp thứ 2: có 2 phân lớp là 2s và 2p
Lời giải chi tiết:
– Lớp thứ nhất: có 1 phân lớp là 1s
– Lớp thứ 2: có 2 phân lớp là 2s và 2p
– Phân lớp s chứa tối đa 2 electron, phân lớp p chứa tối đa 6 electron
=> Cấu hình electron của nguyên tố X: 1s22s22p4
=> Nguyên tố X có 8 electron
=> Số hiệu nguyên tử của X: Z = 8
Bài tập 3
|
Bài 3: Ở trạng thái cơ bản, nguyên tử của những nguyên tố nào dưới đây có electron độc thân?
a) Boron
b) Oxygen
c) Phosphorus
d) Chlorine
|
Phương pháp giải:
Bước 1: Xác định số electron
Bước 2: Viết thứ tự các lớp và phân lớp electron theo chiều tăng dần của năng lượng:
1s 2s 2p 3s 3p 4s 3d 4p
Bước 3: Điền các electron vào các phân lớp theo nguyên lí vững bền cho đến electron cuối cùng
Bước 4: Xác định số electron độc thân
Lời giải chi tiết:
a) Boron (Z = 5): 1s22s22p1 => Có 1 electron độc thân
b) Oxygen (Z = 8): 1s22s22p4 => Có 2 electron độc thân
c) Phosphorus (Z = 15): 1s22s22p63s23p3 => Có 3 electron độc thân
d) Chlorine (Z = 17): 1s22s22p63s23p5 => Có 1 electron độc thân
Bài tập 4
| Bài 4: Viết cấu hình electron nguyên tử của các nguyên tố: carbon (Z = 6), sodium (Z = 11) và oxygen (Z = 8). Cho biết số electron lớp ngoài cùng trong nguyên tử của các nguyên tố trên. Chúng là kim loại, phi kim hay khí hiếm |
Phương pháp giải:
Bước 1: Xác định số electron
Bước 2: Viết thứ tự các lớp và phân lớp electron theo chiều tăng dần của năng lượng:
1s 2s 2p 3s 3p 4s 3d 4p
Bước 3: Điền các electron vào các phân lớp theo nguyên lí vững bền cho đến electron cuối cùng
Bước 4: Xác định số electron ở lớp ngoài cùng
+ Các nguyên tử có 1, 2, 3 electron ở lớp ngoài cùng là các nguyên tử của nguyên tố kim loại
+ Các nguyên tử có 5, 6, 7 electron ở lớp ngoài cùng thường là nguyên tử của các nguyên tố phi kim
+ Các nguyên tử có 4 electron ở lớp ngoài cùng có thể là nguyên tử của nguyên tố kim loại hoặc phi kim
+ Nguyên tử có 8 electron ở lớp ngoài cùng là nguyên tử của nguyên tố khí hiếm
Lời giải chi tiết:
– Nguyên tố Carbon (Z = 6): 1s22s22p2 => Có 4 electron ở lớp ngoài cùng, là nguyên tố phi kim
– Nguyên tố Sodium (Z = 11): 1s22s22p63s1 => Có 1 electron ở lớp ngoài cùng, là nguyên tố kim loại
– Nguyên tố Oxygen (Z = 8): 1s22s22p4 => Có 6 electron ở lớp ngoài cùng, là nguyên tố phi kim
 HỌC NGAY
Môn Toán học Lớp 12SGK Toán lớp 12 SGK Toán 12 Nâng cao SBT Toán lớp 12 SBT Toán lớp 12 Nâng cao Đề thi, đề kiểm tra Toán lớp 12 SGK Toán – Kết nối tri thức SGK Toán – Chân trời sáng tạo SGK Toán – Cánh diềuMôn Ngữ văn Lớp 12Soạn văn 12 siêu ngắn Soạn văn 12 chi tiết Tác giả – Tác phẩm lớp 12 Văn mẫu 12 Luyện dạng đọc hiểu Đề thi, đề kiểm tra Ngữ Văn 12 mới Bài tập trắc nghiệm Văn 12 Soạn văn – Kết nối tri thức Soạn văn – Cánh diều Xem thêmMôn Tiếng Anh Lớp 12Bài tập trắc nghiệm Tiếng Anh 12 mới Bài tập trắc nghiệm Tiếng Anh 12 Đề thi, đề kiểm tra Tiếng Anh 12 mới Tiếng Anh – Global Success Tiếng Anh – Friends Global Tiếng Anh – iLearn Smart World Tiếng Anh – Bright Tiếng Anh – English Discovery SGK Tiếng Anh 12 Mới Xem thêmMôn Vật lí Lớp 12SGK Vật lí lớp 12 SGK Vật lí lớp 12 Nâng cao SBT Vật lí lớp 12 Bài tập trắc nghiệm Lí 12 Đề thi, kiểm tra Lí lớp 12 SGK Vật Lí – Kết nối tri thức SGK Vật Lí – Cánh diều SGK Vật Lí – Chân trời sáng tạoMôn Hóa học Lớp 12SGK Hóa lớp 12 SGK Hóa học lớp 12 Nâng cao SBT Hóa lớp 12 Bài tập trắc nghiệm Hóa 12 Đề thi, đề kiểm tra Hóa lớp 12 SGK Hóa – Kết nối tri thức SGK Hóa – Cánh diều SGK Hóa – Chân trời sáng tạoMôn Sinh học Lớp 12SGK Sinh lớp 12 SGK Sinh lớp 12 Nâng cao SBT Sinh lớp 12 Bài tập trắc nghiệm Sinh 12 Đề thi, đề kiểm tra Sinh lớp 12 SGK Sinh – Kết nối tri thức SGK Sinh – Cánh diều SGK Sinh – Chân trời sáng tạoMôn Lịch sử Lớp 12Tập bản đồ Lịch sử lớp 12 Đề thi, đề kiểm tra Lịch sử 12 SGK Lịch sử lớp 12 SBT Lịch sử lớp 12Môn Địa lí Lớp 12SGK Địa lí lớp 12 SBT Địa lí lớp 12 Tập bản đồ Địa lí lớp 12 Đề thi, kiểm tra Địa lí lớp 12Môn GDCD Lớp 12SGK GDCDMôn Công nghệ Lớp 12SGK Công nghệ 12Môn Tin học Lớp 12SGK Tin học lớp 12
HỌC NGAY
Môn Toán học Lớp 12SGK Toán lớp 12 SGK Toán 12 Nâng cao SBT Toán lớp 12 SBT Toán lớp 12 Nâng cao Đề thi, đề kiểm tra Toán lớp 12 SGK Toán – Kết nối tri thức SGK Toán – Chân trời sáng tạo SGK Toán – Cánh diềuMôn Ngữ văn Lớp 12Soạn văn 12 siêu ngắn Soạn văn 12 chi tiết Tác giả – Tác phẩm lớp 12 Văn mẫu 12 Luyện dạng đọc hiểu Đề thi, đề kiểm tra Ngữ Văn 12 mới Bài tập trắc nghiệm Văn 12 Soạn văn – Kết nối tri thức Soạn văn – Cánh diều Xem thêmMôn Tiếng Anh Lớp 12Bài tập trắc nghiệm Tiếng Anh 12 mới Bài tập trắc nghiệm Tiếng Anh 12 Đề thi, đề kiểm tra Tiếng Anh 12 mới Tiếng Anh – Global Success Tiếng Anh – Friends Global Tiếng Anh – iLearn Smart World Tiếng Anh – Bright Tiếng Anh – English Discovery SGK Tiếng Anh 12 Mới Xem thêmMôn Vật lí Lớp 12SGK Vật lí lớp 12 SGK Vật lí lớp 12 Nâng cao SBT Vật lí lớp 12 Bài tập trắc nghiệm Lí 12 Đề thi, kiểm tra Lí lớp 12 SGK Vật Lí – Kết nối tri thức SGK Vật Lí – Cánh diều SGK Vật Lí – Chân trời sáng tạoMôn Hóa học Lớp 12SGK Hóa lớp 12 SGK Hóa học lớp 12 Nâng cao SBT Hóa lớp 12 Bài tập trắc nghiệm Hóa 12 Đề thi, đề kiểm tra Hóa lớp 12 SGK Hóa – Kết nối tri thức SGK Hóa – Cánh diều SGK Hóa – Chân trời sáng tạoMôn Sinh học Lớp 12SGK Sinh lớp 12 SGK Sinh lớp 12 Nâng cao SBT Sinh lớp 12 Bài tập trắc nghiệm Sinh 12 Đề thi, đề kiểm tra Sinh lớp 12 SGK Sinh – Kết nối tri thức SGK Sinh – Cánh diều SGK Sinh – Chân trời sáng tạoMôn Lịch sử Lớp 12Tập bản đồ Lịch sử lớp 12 Đề thi, đề kiểm tra Lịch sử 12 SGK Lịch sử lớp 12 SBT Lịch sử lớp 12Môn Địa lí Lớp 12SGK Địa lí lớp 12 SBT Địa lí lớp 12 Tập bản đồ Địa lí lớp 12 Đề thi, kiểm tra Địa lí lớp 12Môn GDCD Lớp 12SGK GDCDMôn Công nghệ Lớp 12SGK Công nghệ 12Môn Tin học Lớp 12SGK Tin học lớp 12 HỌC NGAY
Môn Toán học Lớp 11Đề thi, đề kiểm tra Toán – Kết nối tri thức Đề thi, đề kiểm tra Toán – Chân trời sáng tạo Đề thi, đề kiểm tra Toán – Cánh diều SGK Toán – Kết nối tri thức SGK Toán – Cánh diều SGK Toán – Chân trời sáng tạo SGK Toán 11 – Cùng khám phá Chuyên đề học tập Toán – Kết nối tri thức Chuyên đề học tập Toán – Cánh diều Xem thêmMôn Ngữ văn Lớp 11Văn mẫu – Kết nối tri thức Văn mẫu – Cánh diều Văn mẫu – Chân trời sáng tạo Đề thi, đề kiểm tra Văn – Kết nối tri thức Đề thi, đề kiểm tra Văn – Cánh diều Đề thi, đề kiểm tra Văn – Chân trời sáng tạo Tóm tắt, bố cục Văn – Kết nối tri thức Tóm tắt, bố cục Văn – Cánh diều Tóm tắt, bố cục Văn – Chân trời sáng tạo Xem thêmMôn Tiếng Anh Lớp 11Bài tập trắc nghiệm Tiếng Anh – Friends Global Bài tập trắc nghiệm Tiếng Anh – iLearn Smart World Đề thi, đề kiểm tra Tiếng Anh – Global Success Đề thi, đề kiểm tra Tiếng Anh – Friends Global Đề thi, đề kiểm tra Tiếng Anh – iLearn Smart World Đề thi, đề kiểm tra Tiếng Anh – Bright Đề thi, đề kiểm tra Tiếng Anh – English Discovery SBT Tiếng Anh lớp 11 mới Đề thi, đề kiểm tra Tiếng Anh 11 mới Xem thêmMôn Vật lí Lớp 11Đề thi, đề kiểm tra Vật lí – Cánh diều Đề thi, đề kiểm tra Vật lí – Chân trời sáng tạo Bài tập trắc nghiệm Lí – Kết nối tri thức Bài tập trắc nghiệm Lí – Cánh diều Bài tập trắc nghiệm Lí – Chân trời sáng tạo SGK Vật Lí – Kết nối tri thức SGK Vật Lí – Cánh diều SGK Vật Lí – Chân trời sáng tạo Chuyên đề học tập Lí – Kết nối tri thức Xem thêmMôn Hóa học Lớp 11Đề thi, kiểm tra Hóa – Cánh diều Đề thi, kiểm tra Hóa – Chân trời sáng tạo Bài tập trắc nghiệm Hóa – Kết nối tri thức Bài tập trắc nghiệm Hóa – Cánh diều Bài tập trắc nghiệm Hóa – Chân trời sáng tạo SBT Hóa – Chân trời sáng tạo Lý thuyết Hóa 11 Đề thi, kiểm tra Hóa – Kết nối tri thức SGK Hóa học – Kết nối tri thức Xem thêmMôn Sinh học Lớp 11Đề thi, kiểm tra Sinh – Chân trời sáng tạo Đề thi, kiểm tra Sinh – Cánh diều Bài tập trắc nghiệm Sinh – Kết nối tri thức Bài tập trắc nghiệm Sinh – Cánh diều Bài tập trắc nghiệm Sinh – Chân trời sáng tạo SGK Sinh – Kết nối tri thức SGK Sinh – Cánh diều SGK Sinh – Chân trời sáng tạo Chuyên đề học tập Sinh – Kết nối tri thức Xem thêmMôn Lịch sử Lớp 11SGK Lịch sử – Kết nối tri thức SGK Lịch sử – Chân trời sáng tạo SGK Lịch sử – Cánh diều Đề thi, kiểm tra Lịch sử lớp 11Môn Địa lí Lớp 11SGK Địa lí – Kết nối tri thức SGK Địa lí – Chân trời sáng tạo Đề thi, kiểm tra Địa lí lớp 11 SGK Địa lí – Cánh diềuMôn GD kinh tế và pháp luật Lớp 11SGK Giáo dục kinh tế và pháp luật – Kết nối tri thức SGK Giáo dục kinh tế và pháp luật – Chân trời sáng tạo SGK Giáo dục kinh tế và pháp luật – Cánh diềuMôn HĐ trải nghiệm, hướng nghiệp Lớp 11SGK Hoạt động trải nghiệm, hướng nghiệp – Kết nối tri thức SGK Hoạt động trải nghiệm, hướng nghiệp – Cánh diều SGK Hoạt động trải nghiệm, hướng nghiệp – Chân trời sáng tạo Bản 1 SGK Hoạt động trải nghiệm, hướng nghiệp – Chân trời sáng tạo Bản 2Môn Giáo dục thể chất Lớp 11SGK Giáo dục thể chất – Kết nối tri thức SGK Giáo dục thể chất – Cánh diềuMôn GD Quốc phòng và An ninh Lớp 11SGK Giáo dục quốc phòng và an ninh – Kết nối tri thức SGK Giáo dục quốc phòng và an ninh – Cánh diều
HỌC NGAY
Môn Toán học Lớp 11Đề thi, đề kiểm tra Toán – Kết nối tri thức Đề thi, đề kiểm tra Toán – Chân trời sáng tạo Đề thi, đề kiểm tra Toán – Cánh diều SGK Toán – Kết nối tri thức SGK Toán – Cánh diều SGK Toán – Chân trời sáng tạo SGK Toán 11 – Cùng khám phá Chuyên đề học tập Toán – Kết nối tri thức Chuyên đề học tập Toán – Cánh diều Xem thêmMôn Ngữ văn Lớp 11Văn mẫu – Kết nối tri thức Văn mẫu – Cánh diều Văn mẫu – Chân trời sáng tạo Đề thi, đề kiểm tra Văn – Kết nối tri thức Đề thi, đề kiểm tra Văn – Cánh diều Đề thi, đề kiểm tra Văn – Chân trời sáng tạo Tóm tắt, bố cục Văn – Kết nối tri thức Tóm tắt, bố cục Văn – Cánh diều Tóm tắt, bố cục Văn – Chân trời sáng tạo Xem thêmMôn Tiếng Anh Lớp 11Bài tập trắc nghiệm Tiếng Anh – Friends Global Bài tập trắc nghiệm Tiếng Anh – iLearn Smart World Đề thi, đề kiểm tra Tiếng Anh – Global Success Đề thi, đề kiểm tra Tiếng Anh – Friends Global Đề thi, đề kiểm tra Tiếng Anh – iLearn Smart World Đề thi, đề kiểm tra Tiếng Anh – Bright Đề thi, đề kiểm tra Tiếng Anh – English Discovery SBT Tiếng Anh lớp 11 mới Đề thi, đề kiểm tra Tiếng Anh 11 mới Xem thêmMôn Vật lí Lớp 11Đề thi, đề kiểm tra Vật lí – Cánh diều Đề thi, đề kiểm tra Vật lí – Chân trời sáng tạo Bài tập trắc nghiệm Lí – Kết nối tri thức Bài tập trắc nghiệm Lí – Cánh diều Bài tập trắc nghiệm Lí – Chân trời sáng tạo SGK Vật Lí – Kết nối tri thức SGK Vật Lí – Cánh diều SGK Vật Lí – Chân trời sáng tạo Chuyên đề học tập Lí – Kết nối tri thức Xem thêmMôn Hóa học Lớp 11Đề thi, kiểm tra Hóa – Cánh diều Đề thi, kiểm tra Hóa – Chân trời sáng tạo Bài tập trắc nghiệm Hóa – Kết nối tri thức Bài tập trắc nghiệm Hóa – Cánh diều Bài tập trắc nghiệm Hóa – Chân trời sáng tạo SBT Hóa – Chân trời sáng tạo Lý thuyết Hóa 11 Đề thi, kiểm tra Hóa – Kết nối tri thức SGK Hóa học – Kết nối tri thức Xem thêmMôn Sinh học Lớp 11Đề thi, kiểm tra Sinh – Chân trời sáng tạo Đề thi, kiểm tra Sinh – Cánh diều Bài tập trắc nghiệm Sinh – Kết nối tri thức Bài tập trắc nghiệm Sinh – Cánh diều Bài tập trắc nghiệm Sinh – Chân trời sáng tạo SGK Sinh – Kết nối tri thức SGK Sinh – Cánh diều SGK Sinh – Chân trời sáng tạo Chuyên đề học tập Sinh – Kết nối tri thức Xem thêmMôn Lịch sử Lớp 11SGK Lịch sử – Kết nối tri thức SGK Lịch sử – Chân trời sáng tạo SGK Lịch sử – Cánh diều Đề thi, kiểm tra Lịch sử lớp 11Môn Địa lí Lớp 11SGK Địa lí – Kết nối tri thức SGK Địa lí – Chân trời sáng tạo Đề thi, kiểm tra Địa lí lớp 11 SGK Địa lí – Cánh diềuMôn GD kinh tế và pháp luật Lớp 11SGK Giáo dục kinh tế và pháp luật – Kết nối tri thức SGK Giáo dục kinh tế và pháp luật – Chân trời sáng tạo SGK Giáo dục kinh tế và pháp luật – Cánh diềuMôn HĐ trải nghiệm, hướng nghiệp Lớp 11SGK Hoạt động trải nghiệm, hướng nghiệp – Kết nối tri thức SGK Hoạt động trải nghiệm, hướng nghiệp – Cánh diều SGK Hoạt động trải nghiệm, hướng nghiệp – Chân trời sáng tạo Bản 1 SGK Hoạt động trải nghiệm, hướng nghiệp – Chân trời sáng tạo Bản 2Môn Giáo dục thể chất Lớp 11SGK Giáo dục thể chất – Kết nối tri thức SGK Giáo dục thể chất – Cánh diềuMôn GD Quốc phòng và An ninh Lớp 11SGK Giáo dục quốc phòng và an ninh – Kết nối tri thức SGK Giáo dục quốc phòng và an ninh – Cánh diều HỌC NGAY
Môn Toán học Lớp 10Đề thi, đề kiểm tra Toán – Cánh diều Lý thuyết Toán 10 SBT Toán – Chân trời sáng tạo SBT Toán – Cánh diều Chuyên đề học tập Toán – Kết nối tri thức Chuyên đề học tập Toán – Chân trời sáng tạo Chuyên đề học tập Toán – Cánh diều Đề thi, đề kiểm tra Toán – Kết nối tri thức Đề thi, đề kiểm tra Toán – Chân trời sáng tạo Xem thêmMôn Ngữ văn Lớp 10SBT Văn – Chân trời sáng tạo SBT Văn – Cánh diều Chuyên đề học tập Văn – Kết nối tri thức Chuyên đề học tập Văn – Chân trời sáng tạo Chuyên đề học tập Văn – Cánh diều Soạn văn – Kết nối tri thức – siêu ngắn Đề thi, đề kiểm tra Văn – Kết nối tri thức Soạn văn – Kết nối tri thức – chi tiết Đề thi, đề kiểm tra Văn – Cánh diều Xem thêmMôn Tiếng Anh Lớp 10Bài tập trắc nghiệm Tiếng Anh – Global Success Bài tập trắc nghiệm Tiếng Anh – Friends Global Bài tập trắc nghiệm Tiếng Anh – iLearn Smart World Đề thi, đề kiểm tra Tiếng Anh – Global Success Đề thi, đề kiểm tra Tiếng Anh – Friends Global Tiếng Anh – Global Success Đề thi, đề kiểm tra Tiếng Anh – iLearn Smart World Tiếng Anh – Friends Global Đề thi, đề kiểm tra Tiếng Anh – Bright Xem thêmMôn Vật lí Lớp 10Đề thi, đề kiểm tra Vật lí – Cánh diều Chuyên đề học tập Lí – Kết nối tri thức Chuyên đề học tập Lí – Cánh diều Chuyên đề học tập Lí – Chân trời sáng tạo Lý thuyết Vật lí 10 SBT Vật lí – Chân trời sáng tạo SBT Vật lí – Cánh diều Bài tập trắc nghiệm Lí – Kết nối tri thức Bài tập trắc nghiệm Lí – Chân trời sáng tạo Xem thêmMôn Hóa học Lớp 10Bài tập trắc nghiệm Hóa – Cánh diều Đề thi, kiểm tra Hóa – Kết nối tri thức Đề thi, kiểm tra Hóa – Chân trời sáng tạo Đề thi, kiểm tra Hóa – Cánh diều Lý thuyết Hóa 10 SGK Hóa – Kết nối tri thức SGK Hóa – Chân trời sáng tạo SGK Hóa – Cánh diều SBT Hóa – Kết nối tri thức Xem thêmMôn Sinh học Lớp 10Đề thi, kiểm tra Sinh – Kết nối tri thức Đề thi, kiểm tra Sinh – Chân trời sáng tạo Đề thi, kiểm tra Sinh – Cánh diều Lý thuyết Sinh 10 SBT Sinh – Chân trời sáng tạo SBT Sinh – Cánh diều Chuyên đề học tập Sinh – Kết nối tri thức Chuyên đề học tập Sinh – Chân trời sáng tạo Bài tập trắc nghiệm Sinh – Kết nối tri thức Xem thêmMôn Lịch sử Lớp 10SGK Lịch sử – Kết nối tri thức SGK Lịch sử – Chân trời sáng tạo SGK Lịch sử – Cánh Diều SBT Lịch sử – Kết nối tri thức SBT Lịch sử – Chân trời sáng tạo SBT Lịch sử – Cánh Diều Chuyên đề học tập Lịch sử – Kết nối tri thức Đề thi, đề kiểm tra Lịch sử – Kết nối tri thức Đề thi, đề kiểm tra Lịch sử lớp 10 – Chân trời sáng tạo Xem thêmMôn Địa lí Lớp 10SGK Địa lí – Kết nối tri thức SGK Địa lí – Cánh Diều SGK Địa lí – Chân trời sáng tạo SBT Địa lí – Kết nối tri thức SBT Địa lí – Chân trời sáng tạo Đề thi, đề kiểm tra Địa lí – Kết nối tri thức Đề thi, đề kiểm tra Địa lí lớp 10 – Chân trời sáng tạo Đề thi, đề kiểm tra Địa lí – Kết nối tri thứcMôn GDCD Lớp 10SGK Giáo dục kinh tế và pháp luật – KNTT SGK Giáo dục kinh tế và pháp luật – CTST SGK Giáo dục kinh tế và pháp luật – Cánh diềuMôn Tin học Lớp 10SGK Tin học – Kết nối tri thức SGK Tin học – Cánh Diều SBT Tin học – Kết nối tri thứcMôn HĐ trải nghiệm, hướng nghiệp Lớp 10SGK Hoạt động trải nghiệm, hướng nghiệp – Kết nối tri thức SGK Hoạt động trải nghiệm, hướng nghiệp – Chân trời sáng tạo SGK Hoạt động trải nghiệm, hướng nghiệp – Cánh DiềuMôn Giáo dục thể chất Lớp 10SGK Giáo dục thể chất – Kết nối tri thức SGK Giáo dục thể chất – Cánh diềuMôn GD Quốc phòng và An ninh Lớp 10SGK Giáo dục quốc phòng và an ninh – Kết nối tri thức SGK Giáo dục quốc phòng và an ninh – Cánh diều
HỌC NGAY
Môn Toán học Lớp 10Đề thi, đề kiểm tra Toán – Cánh diều Lý thuyết Toán 10 SBT Toán – Chân trời sáng tạo SBT Toán – Cánh diều Chuyên đề học tập Toán – Kết nối tri thức Chuyên đề học tập Toán – Chân trời sáng tạo Chuyên đề học tập Toán – Cánh diều Đề thi, đề kiểm tra Toán – Kết nối tri thức Đề thi, đề kiểm tra Toán – Chân trời sáng tạo Xem thêmMôn Ngữ văn Lớp 10SBT Văn – Chân trời sáng tạo SBT Văn – Cánh diều Chuyên đề học tập Văn – Kết nối tri thức Chuyên đề học tập Văn – Chân trời sáng tạo Chuyên đề học tập Văn – Cánh diều Soạn văn – Kết nối tri thức – siêu ngắn Đề thi, đề kiểm tra Văn – Kết nối tri thức Soạn văn – Kết nối tri thức – chi tiết Đề thi, đề kiểm tra Văn – Cánh diều Xem thêmMôn Tiếng Anh Lớp 10Bài tập trắc nghiệm Tiếng Anh – Global Success Bài tập trắc nghiệm Tiếng Anh – Friends Global Bài tập trắc nghiệm Tiếng Anh – iLearn Smart World Đề thi, đề kiểm tra Tiếng Anh – Global Success Đề thi, đề kiểm tra Tiếng Anh – Friends Global Tiếng Anh – Global Success Đề thi, đề kiểm tra Tiếng Anh – iLearn Smart World Tiếng Anh – Friends Global Đề thi, đề kiểm tra Tiếng Anh – Bright Xem thêmMôn Vật lí Lớp 10Đề thi, đề kiểm tra Vật lí – Cánh diều Chuyên đề học tập Lí – Kết nối tri thức Chuyên đề học tập Lí – Cánh diều Chuyên đề học tập Lí – Chân trời sáng tạo Lý thuyết Vật lí 10 SBT Vật lí – Chân trời sáng tạo SBT Vật lí – Cánh diều Bài tập trắc nghiệm Lí – Kết nối tri thức Bài tập trắc nghiệm Lí – Chân trời sáng tạo Xem thêmMôn Hóa học Lớp 10Bài tập trắc nghiệm Hóa – Cánh diều Đề thi, kiểm tra Hóa – Kết nối tri thức Đề thi, kiểm tra Hóa – Chân trời sáng tạo Đề thi, kiểm tra Hóa – Cánh diều Lý thuyết Hóa 10 SGK Hóa – Kết nối tri thức SGK Hóa – Chân trời sáng tạo SGK Hóa – Cánh diều SBT Hóa – Kết nối tri thức Xem thêmMôn Sinh học Lớp 10Đề thi, kiểm tra Sinh – Kết nối tri thức Đề thi, kiểm tra Sinh – Chân trời sáng tạo Đề thi, kiểm tra Sinh – Cánh diều Lý thuyết Sinh 10 SBT Sinh – Chân trời sáng tạo SBT Sinh – Cánh diều Chuyên đề học tập Sinh – Kết nối tri thức Chuyên đề học tập Sinh – Chân trời sáng tạo Bài tập trắc nghiệm Sinh – Kết nối tri thức Xem thêmMôn Lịch sử Lớp 10SGK Lịch sử – Kết nối tri thức SGK Lịch sử – Chân trời sáng tạo SGK Lịch sử – Cánh Diều SBT Lịch sử – Kết nối tri thức SBT Lịch sử – Chân trời sáng tạo SBT Lịch sử – Cánh Diều Chuyên đề học tập Lịch sử – Kết nối tri thức Đề thi, đề kiểm tra Lịch sử – Kết nối tri thức Đề thi, đề kiểm tra Lịch sử lớp 10 – Chân trời sáng tạo Xem thêmMôn Địa lí Lớp 10SGK Địa lí – Kết nối tri thức SGK Địa lí – Cánh Diều SGK Địa lí – Chân trời sáng tạo SBT Địa lí – Kết nối tri thức SBT Địa lí – Chân trời sáng tạo Đề thi, đề kiểm tra Địa lí – Kết nối tri thức Đề thi, đề kiểm tra Địa lí lớp 10 – Chân trời sáng tạo Đề thi, đề kiểm tra Địa lí – Kết nối tri thứcMôn GDCD Lớp 10SGK Giáo dục kinh tế và pháp luật – KNTT SGK Giáo dục kinh tế và pháp luật – CTST SGK Giáo dục kinh tế và pháp luật – Cánh diềuMôn Tin học Lớp 10SGK Tin học – Kết nối tri thức SGK Tin học – Cánh Diều SBT Tin học – Kết nối tri thứcMôn HĐ trải nghiệm, hướng nghiệp Lớp 10SGK Hoạt động trải nghiệm, hướng nghiệp – Kết nối tri thức SGK Hoạt động trải nghiệm, hướng nghiệp – Chân trời sáng tạo SGK Hoạt động trải nghiệm, hướng nghiệp – Cánh DiềuMôn Giáo dục thể chất Lớp 10SGK Giáo dục thể chất – Kết nối tri thức SGK Giáo dục thể chất – Cánh diềuMôn GD Quốc phòng và An ninh Lớp 10SGK Giáo dục quốc phòng và an ninh – Kết nối tri thức SGK Giáo dục quốc phòng và an ninh – Cánh diều HỌC NGAY
Môn Toán học Lớp 9SGK Toán lớp 9 SBT Toán lớp 9 Vở bài tập Toán 9 Bài tập trắc nghiệm Toán 9 Tài liệu Dạy – học Toán 9 Đề thi, đề kiểm tra Toán lớp 9 Đề thi vào 10 môn Toán SGK Toán – Kết nối tri thức SGK Toán – Chân trời sáng tạo Xem thêmMôn Ngữ văn Lớp 9Soạn văn 9 siêu ngắn Soạn văn 9 chi tiết Tác giả – Tác phẩm văn 9 Văn mẫu lớp 9 Vở bài tập Ngữ văn lớp 9 Bài tập trắc nghiệm Văn 9 Đề thi vào 10 môn Văn Đề thi, đề kiểm tra Văn 9 Soạn văn – Kết nối tri thức Xem thêmMôn Tiếng Anh Lớp 9Tiếng Anh – English Discovery Tiếng Anh – Friends Plus Tiếng Anh – iLearn Smart World Tiếng Anh – Right on! SGK Tiếng Anh lớp 9 Mới SGK Tiếng Anh lớp 9 SBT Tiếng Anh lớp 9 mới Vở bài tập Tiếng Anh 9 Bài tập trắc nghiệm Tiếng Anh 9 mới Xem thêmMôn Vật lí Lớp 9SGK Vật lí lớp 9 SBT Vật lí lớp 9 Vở bài tập Vật lí 9 Bài tập trắc nghiệm Lí 9 Tài liệu Dạy – Học Vật lí 9 Đề thi, kiểm tra Lí lớp 9Môn Hóa học Lớp 9SGK Hóa lớp 9 SBT Hóa lớp 9 Vở bài tập Hoá học 9 Bài tập trắc nghiệm Hóa 9 Tài liệu Dạy – học Hóa học 9 Đề thi, đề kiểm tra Hóa lớp 9Môn Sinh học Lớp 9SGK Sinh lớp 9 SBT Sinh lớp 9 Vở bài tập Sinh học 9 Đề thi, đề kiểm tra Sinh lớp 9 Bài tập trắc nghiệm Sinh 9 Đề thi, đề kiểm tra Sinh lớp 9Môn Lịch sử Lớp 9SGK Lịch sử lớp 9 VBT Lịch sử lớp 9 Tập bản đồ Lịch sử lớp 9 SBT Lịch sử lớp 9 Đề thi, kiểm tra Lịch sử lớp 9Môn Địa lí Lớp 9Đề thi, kiểm tra Địa lí lớp 9 SGK Địa lí lớp 9 SBT Địa lí lớp 9 VBT Địa lí lớp 9 Tập bản đồ Địa lí lớp 9Môn Công nghệ Lớp 9SGK Công nghệ 9Môn Tin học Lớp 9SGK Tin học lớp 9Môn Khoa học tự nhiên Lớp 9SGK Khoa học tự nhiên – Cánh diều SGK Khoa học tự nhiên – Chân trời sáng tạo SGK Khoa học tự nhiên – Kết nối tri thứcMôn Âm nhạc và mỹ thuật Lớp 9Âm nhạc và mỹ thuật lớp 9
HỌC NGAY
Môn Toán học Lớp 9SGK Toán lớp 9 SBT Toán lớp 9 Vở bài tập Toán 9 Bài tập trắc nghiệm Toán 9 Tài liệu Dạy – học Toán 9 Đề thi, đề kiểm tra Toán lớp 9 Đề thi vào 10 môn Toán SGK Toán – Kết nối tri thức SGK Toán – Chân trời sáng tạo Xem thêmMôn Ngữ văn Lớp 9Soạn văn 9 siêu ngắn Soạn văn 9 chi tiết Tác giả – Tác phẩm văn 9 Văn mẫu lớp 9 Vở bài tập Ngữ văn lớp 9 Bài tập trắc nghiệm Văn 9 Đề thi vào 10 môn Văn Đề thi, đề kiểm tra Văn 9 Soạn văn – Kết nối tri thức Xem thêmMôn Tiếng Anh Lớp 9Tiếng Anh – English Discovery Tiếng Anh – Friends Plus Tiếng Anh – iLearn Smart World Tiếng Anh – Right on! SGK Tiếng Anh lớp 9 Mới SGK Tiếng Anh lớp 9 SBT Tiếng Anh lớp 9 mới Vở bài tập Tiếng Anh 9 Bài tập trắc nghiệm Tiếng Anh 9 mới Xem thêmMôn Vật lí Lớp 9SGK Vật lí lớp 9 SBT Vật lí lớp 9 Vở bài tập Vật lí 9 Bài tập trắc nghiệm Lí 9 Tài liệu Dạy – Học Vật lí 9 Đề thi, kiểm tra Lí lớp 9Môn Hóa học Lớp 9SGK Hóa lớp 9 SBT Hóa lớp 9 Vở bài tập Hoá học 9 Bài tập trắc nghiệm Hóa 9 Tài liệu Dạy – học Hóa học 9 Đề thi, đề kiểm tra Hóa lớp 9Môn Sinh học Lớp 9SGK Sinh lớp 9 SBT Sinh lớp 9 Vở bài tập Sinh học 9 Đề thi, đề kiểm tra Sinh lớp 9 Bài tập trắc nghiệm Sinh 9 Đề thi, đề kiểm tra Sinh lớp 9Môn Lịch sử Lớp 9SGK Lịch sử lớp 9 VBT Lịch sử lớp 9 Tập bản đồ Lịch sử lớp 9 SBT Lịch sử lớp 9 Đề thi, kiểm tra Lịch sử lớp 9Môn Địa lí Lớp 9Đề thi, kiểm tra Địa lí lớp 9 SGK Địa lí lớp 9 SBT Địa lí lớp 9 VBT Địa lí lớp 9 Tập bản đồ Địa lí lớp 9Môn Công nghệ Lớp 9SGK Công nghệ 9Môn Tin học Lớp 9SGK Tin học lớp 9Môn Khoa học tự nhiên Lớp 9SGK Khoa học tự nhiên – Cánh diều SGK Khoa học tự nhiên – Chân trời sáng tạo SGK Khoa học tự nhiên – Kết nối tri thứcMôn Âm nhạc và mỹ thuật Lớp 9Âm nhạc và mỹ thuật lớp 9 HỌC NGAY
Môn Toán học Lớp 8Lý thuyết Toán 8 Bài tập trắc nghiệm Toán – Kết nối tri thức Bài tập trắc nghiệm Toán – Chân trời sáng tạo Bài tập trắc nghiệm Toán – Cánh diều SGK Toán – Kết nối tri thức SGK Toán – Chân trời sáng tạo SGK Toán – Cánh diều SGK Toán 8 – Cùng khám phá SBT Toán – Kết nối tri thức Xem thêmMôn Ngữ văn Lớp 8Lý thuyết Văn 8 Bài tập trắc nghiệm Văn – Kết nối tri thức Bài tập trắc nghiệm Văn – Cánh diều Bài tập trắc nghiệm Văn – Chân trời sáng tạo Văn mẫu – Kết nối tri thức Soạn văn chi tiết – KNTT Văn mẫu – Chân trời sáng tạo Soạn văn siêu ngắn – KNTT Văn mẫu – Cánh Diều Xem thêmMôn Tiếng Anh Lớp 8Đề thi, đề kiểm tra Tiếng Anh – Friends Plus Đề thi, đề kiểm tra Tiếng Anh – iLearn Smart World Đề thi, đề kiểm tra Tiếng Anh – Right on! Đề thi, đề kiểm tra Tiếng Anh – English Discovery Đề thi, đề kiểm tra Tiếng Anh 8 mới Lý thuyết Tiếng Anh 8 Bài tập trắc nghiệm Tiếng Anh – Friends Plus Bài tập trắc nghiệm Tiếng Anh – iLearn Smart World Đề thi, đề kiểm tra Tiếng Anh – Global Success Xem thêmMôn GDCD Lớp 8Giáo dục công dân – Kết nối tri thức Giáo dục công dân – Chân trời sáng tạo Giáo dục công dân – Cánh diềuMôn Công nghệ Lớp 8SGK Công nghệ – Kết nối tri thức SGK Công nghệ – Chân trời sáng tạo SGK Công nghệ – Cánh diềuMôn HĐ trải nghiệm, hướng nghiệp Lớp 8SGK Hoạt động trải nghiệm, hướng nghiệp – Kết nối tri thức SGK Hoạt động trải nghiệm, hướng nghiệp – Cánh diều SGK Hoạt động trải nghiệm, hướng nghiệp – Chân trời sáng tạo Bản 1 SGK Hoạt động trải nghiệm, hướng nghiệp – Chân trời sáng tạo Bản 2Môn Giáo dục thể chất Lớp 8SGK Giáo dục thể chất – Kết nối tri thức SGK Giáo dục thể chất – Cánh diều SGK Giáo dục thể chất – Chân trời sáng tạoMôn Khoa học tự nhiên Lớp 8SGK Khoa học tự nhiên – Kết nối tri thức SGK Khoa học tự nhiên – Cánh diều SBT KHTN – Kết nối tri thức SBT KHTN – Cánh diều Vở thực hành Khoa học tự nhiên Đề thi, đề kiểm tra KHTN – Kết nối tri thức Đề thi, đề kiểm tra KHTN – Cánh diều Lý thuyết Khoa học tự nhiên 8 Bài tập trắc nghiệm Khoa học tự nhiên – Kết nối tri thức Xem thêmMôn Lịch sử và Địa lí Lớp 8SGK Lịch sử và Địa lí – Kết nối tri thức SGK Lịch sử và Địa lí – Cánh diều SGK Lịch sử và Địa lí – Chân trời sáng tạo Đề thi, kiểm tra Lịch Sử và Địa lí – Kết nối tri thức Đề thi, kiểm tra Lịch sử và Địa lí – Chân trời sáng tạo Đề thi, kiểm tra Lịch Sử và Địa lí – Cánh diều
HỌC NGAY
Môn Toán học Lớp 8Lý thuyết Toán 8 Bài tập trắc nghiệm Toán – Kết nối tri thức Bài tập trắc nghiệm Toán – Chân trời sáng tạo Bài tập trắc nghiệm Toán – Cánh diều SGK Toán – Kết nối tri thức SGK Toán – Chân trời sáng tạo SGK Toán – Cánh diều SGK Toán 8 – Cùng khám phá SBT Toán – Kết nối tri thức Xem thêmMôn Ngữ văn Lớp 8Lý thuyết Văn 8 Bài tập trắc nghiệm Văn – Kết nối tri thức Bài tập trắc nghiệm Văn – Cánh diều Bài tập trắc nghiệm Văn – Chân trời sáng tạo Văn mẫu – Kết nối tri thức Soạn văn chi tiết – KNTT Văn mẫu – Chân trời sáng tạo Soạn văn siêu ngắn – KNTT Văn mẫu – Cánh Diều Xem thêmMôn Tiếng Anh Lớp 8Đề thi, đề kiểm tra Tiếng Anh – Friends Plus Đề thi, đề kiểm tra Tiếng Anh – iLearn Smart World Đề thi, đề kiểm tra Tiếng Anh – Right on! Đề thi, đề kiểm tra Tiếng Anh – English Discovery Đề thi, đề kiểm tra Tiếng Anh 8 mới Lý thuyết Tiếng Anh 8 Bài tập trắc nghiệm Tiếng Anh – Friends Plus Bài tập trắc nghiệm Tiếng Anh – iLearn Smart World Đề thi, đề kiểm tra Tiếng Anh – Global Success Xem thêmMôn GDCD Lớp 8Giáo dục công dân – Kết nối tri thức Giáo dục công dân – Chân trời sáng tạo Giáo dục công dân – Cánh diềuMôn Công nghệ Lớp 8SGK Công nghệ – Kết nối tri thức SGK Công nghệ – Chân trời sáng tạo SGK Công nghệ – Cánh diềuMôn HĐ trải nghiệm, hướng nghiệp Lớp 8SGK Hoạt động trải nghiệm, hướng nghiệp – Kết nối tri thức SGK Hoạt động trải nghiệm, hướng nghiệp – Cánh diều SGK Hoạt động trải nghiệm, hướng nghiệp – Chân trời sáng tạo Bản 1 SGK Hoạt động trải nghiệm, hướng nghiệp – Chân trời sáng tạo Bản 2Môn Giáo dục thể chất Lớp 8SGK Giáo dục thể chất – Kết nối tri thức SGK Giáo dục thể chất – Cánh diều SGK Giáo dục thể chất – Chân trời sáng tạoMôn Khoa học tự nhiên Lớp 8SGK Khoa học tự nhiên – Kết nối tri thức SGK Khoa học tự nhiên – Cánh diều SBT KHTN – Kết nối tri thức SBT KHTN – Cánh diều Vở thực hành Khoa học tự nhiên Đề thi, đề kiểm tra KHTN – Kết nối tri thức Đề thi, đề kiểm tra KHTN – Cánh diều Lý thuyết Khoa học tự nhiên 8 Bài tập trắc nghiệm Khoa học tự nhiên – Kết nối tri thức Xem thêmMôn Lịch sử và Địa lí Lớp 8SGK Lịch sử và Địa lí – Kết nối tri thức SGK Lịch sử và Địa lí – Cánh diều SGK Lịch sử và Địa lí – Chân trời sáng tạo Đề thi, kiểm tra Lịch Sử và Địa lí – Kết nối tri thức Đề thi, kiểm tra Lịch sử và Địa lí – Chân trời sáng tạo Đề thi, kiểm tra Lịch Sử và Địa lí – Cánh diều HỌC NGAY
Môn Toán học Lớp 7Đề thi, đề kiểm tra Toán – Cánh diều Lý thuyết Toán 7 Tài liệu Dạy – học Toán 7 Vở thực hành SGK Toán – Kết nối tri thức SGK Toán – Chân trời sáng tạo SGK Toán – Cánh diều SBT Toán – Kết nối tri thức SBT Toán – Chân trời sáng tạo Xem thêmMôn Ngữ văn Lớp 7SBT Văn – Chân trời sáng tạo Đề thi, đề kiểm tra Văn – Kết nối tri thức Đề thi, đề kiểm tra Văn – Chân trời sáng tạo Đề thi, đề kiểm tra Văn – Cánh diều Bài tập trắc nghiệm Văn – Kết nối tri thức Bài tập trắc nghiệm Văn – Chân trời sáng tạo Bài tập trắc nghiệm Văn – Cánh diều Vở thực hành văn Lý thuyết Văn 7 Xem thêmMôn Tiếng Anh Lớp 7Bài tập trắc nghiệm Tiếng Anh – Friends Plus Bài tập trắc nghiệm Tiếng Anh – iLearn Smart World Đề thi, đề kiểm tra Tiếng Anh – Global Success Đề thi, đề kiểm tra Tiếng Anh – Friends Plus Đề thi, đề kiểm tra Tiếng Anh – iLearn Smart World Đề thi, đề kiểm tra Tiếng Anh – Right on! Đề thi, đề kiểm tra Tiếng Anh – English Discovery Lý thuyết Tiếng Anh 7 Tiếng Anh – Global Success Xem thêmMôn Công nghệ Lớp 7SGK Công nghệ – Kết nối tri thức SGK Công nghệ – Chân trời sáng tạo SGK Công nghệ – Cánh diềuMôn Tin học Lớp 7SGK Tin học – Kết nối tri thức SGK Tin học – Cánh Diều SGK Tin học – Chân trời sáng tạo SBT Tin học – Kết nối tri thứcMôn HĐ trải nghiệm, hướng nghiệp Lớp 7SGK Hoạt động trải nghiệm, hướng nghiệp – Kết nối tri thức SGK Hoạt động trải nghiệm, hướng nghiệp – Cánh Diều SGK Hoạt động trải nghiệm, hướng nghiệp – Chân trời sáng tạoMôn Khoa học tự nhiên Lớp 7Đề thi, đề kiểm tra KHTN – Cánh Diều Vở thực hành Khoa học tự nhiên 7 Lý thuyết Khoa học tự nhiên 7 SGK Khoa học tự nhiên – Kết nối tri thức SGK Khoa học tự nhiên – Chân trời sáng tạo SGK Khoa học tự nhiên – Cánh diều SBT KHTN – Kết nối tri thức SBT KHTN – Chân trời sáng tạo SBT KHTN – Cánh diều Xem thêmMôn Lịch sử và Địa lí Lớp 7SGK Lịch sử và Địa lí – Kết nối tri thức SGK Lịch sử và Địa lí – Chân trời sáng tạo SGK Lịch sử và Địa lí – Cánh Diều SBT Lịch sử và Địa lí – Kết nối tri thức SBT Lịch sử và Địa lí – Chân trời sáng tạo SBT Lịch sử và Địa lí – Cánh diều Đề thi, kiểm tra Lịch sử và Địa lí lớp 7 – Kết nối tri thức Đề thi, kiểm tra Lịch sử và Địa lí lớp 7 – Chân trời sáng tạo
HỌC NGAY
Môn Toán học Lớp 7Đề thi, đề kiểm tra Toán – Cánh diều Lý thuyết Toán 7 Tài liệu Dạy – học Toán 7 Vở thực hành SGK Toán – Kết nối tri thức SGK Toán – Chân trời sáng tạo SGK Toán – Cánh diều SBT Toán – Kết nối tri thức SBT Toán – Chân trời sáng tạo Xem thêmMôn Ngữ văn Lớp 7SBT Văn – Chân trời sáng tạo Đề thi, đề kiểm tra Văn – Kết nối tri thức Đề thi, đề kiểm tra Văn – Chân trời sáng tạo Đề thi, đề kiểm tra Văn – Cánh diều Bài tập trắc nghiệm Văn – Kết nối tri thức Bài tập trắc nghiệm Văn – Chân trời sáng tạo Bài tập trắc nghiệm Văn – Cánh diều Vở thực hành văn Lý thuyết Văn 7 Xem thêmMôn Tiếng Anh Lớp 7Bài tập trắc nghiệm Tiếng Anh – Friends Plus Bài tập trắc nghiệm Tiếng Anh – iLearn Smart World Đề thi, đề kiểm tra Tiếng Anh – Global Success Đề thi, đề kiểm tra Tiếng Anh – Friends Plus Đề thi, đề kiểm tra Tiếng Anh – iLearn Smart World Đề thi, đề kiểm tra Tiếng Anh – Right on! Đề thi, đề kiểm tra Tiếng Anh – English Discovery Lý thuyết Tiếng Anh 7 Tiếng Anh – Global Success Xem thêmMôn Công nghệ Lớp 7SGK Công nghệ – Kết nối tri thức SGK Công nghệ – Chân trời sáng tạo SGK Công nghệ – Cánh diềuMôn Tin học Lớp 7SGK Tin học – Kết nối tri thức SGK Tin học – Cánh Diều SGK Tin học – Chân trời sáng tạo SBT Tin học – Kết nối tri thứcMôn HĐ trải nghiệm, hướng nghiệp Lớp 7SGK Hoạt động trải nghiệm, hướng nghiệp – Kết nối tri thức SGK Hoạt động trải nghiệm, hướng nghiệp – Cánh Diều SGK Hoạt động trải nghiệm, hướng nghiệp – Chân trời sáng tạoMôn Khoa học tự nhiên Lớp 7Đề thi, đề kiểm tra KHTN – Cánh Diều Vở thực hành Khoa học tự nhiên 7 Lý thuyết Khoa học tự nhiên 7 SGK Khoa học tự nhiên – Kết nối tri thức SGK Khoa học tự nhiên – Chân trời sáng tạo SGK Khoa học tự nhiên – Cánh diều SBT KHTN – Kết nối tri thức SBT KHTN – Chân trời sáng tạo SBT KHTN – Cánh diều Xem thêmMôn Lịch sử và Địa lí Lớp 7SGK Lịch sử và Địa lí – Kết nối tri thức SGK Lịch sử và Địa lí – Chân trời sáng tạo SGK Lịch sử và Địa lí – Cánh Diều SBT Lịch sử và Địa lí – Kết nối tri thức SBT Lịch sử và Địa lí – Chân trời sáng tạo SBT Lịch sử và Địa lí – Cánh diều Đề thi, kiểm tra Lịch sử và Địa lí lớp 7 – Kết nối tri thức Đề thi, kiểm tra Lịch sử và Địa lí lớp 7 – Chân trời sáng tạo HỌC NGAY
Môn Toán học Lớp 6Đề thi, đề kiểm tra Toán – Kết nối tri thức Đề thi, đề kiểm tra Toán – Chân trời sáng tạo Đề thi, đề kiểm tra Toán – Cánh diều Vở thực hành Toán 6 SGK Toán – Kết nối tri thức SGK Toán – Chân trời sáng tạo SGK Toán – Cánh diều SBT Toán – Kết nối tri thức SBT Toán – Chân trời sáng tạo Xem thêmMôn Ngữ văn Lớp 6Vở thực hành văn Ôn tập hè Văn lớp 6 Bài tập trắc nghiệm Văn – Cánh diều Bài tập trắc nghiệm Văn – Chân trời sáng tạo Đề thi, đề kiểm tra Văn – Kết nối tri thức Đề thi, đề kiểm tra Văn – Cánh diều Đề thi, đề kiểm tra Văn – Chân trời sáng tạo Soạn văn siêu ngắn – KNTT Văn mẫu 6- Kết nối tri thức Xem thêmMôn Tiếng Anh Lớp 6Bài tập trắc nghiệm Tiếng Anh 6 – English Discovery Đề thi, đề kiểm tra Tiếng Anh – Global Success Đề thi, đề kiểm tra Tiếng Anh – Friends Plus Đề thi, đề kiểm tra Tiếng Anh – iLearn Smart World Đề thi, đề kiểm tra Tiếng Anh – Right on! Đề thi, đề kiểm tra Tiếng Anh – English Discovery Ôn tập hè Tiếng Anh lớp 6 Bài tập trắc nghiệm Tiếng Anh – Global Success Bài tập trắc nghiệm Tiếng Anh – Friends Plus Xem thêmMôn GDCD Lớp 6SGK GDCD – CTST SGK GDCD – Cánh Diều SBT GDCD – Kết nối tri thức SBT GDCD – Chân trời sáng tạo SBT GDCD – Cánh diều SGK GDCD – KNTTMôn Công nghệ Lớp 6Công nghệ – Kết nối tri thức Công nghệ – Cánh Diều Công nghệ – Chân trời sáng tạo SBT Công nghệ – Kết nối tri thức SBT Công nghệ – Cánh diều SBT Công nghệ – Chân trời sáng tạoMôn Tin học Lớp 6Tin học – Kết nối tri thức + chân trời sáng tạo Tin học – Cánh Diều SBT Tin học – Kết nối tri thức SBT Tin học – Cánh DiềuMôn HĐ trải nghiệm, hướng nghiệp Lớp 6SGK Trải nghiệm, hướng nghiệp – Kết nối tri thức SGK Trải nghiệm, hướng nghiệp – Chân trời sáng tạo SGK Trải nghiệm, hướng nghiệp – Cánh diều SBT Trải nghiệm, hướng nghiệp – Kết nối tri thức SBT Trải nghiệm, hướng nghiệp – Chân trời sáng tạo Thực hành Trải nghiệm, hướng nghiệp – Cánh diềuMôn Khoa học tự nhiên Lớp 6Đề thi, đề kiểm tra KHTN – Cánh diều Vở thực hành Khoa học tự nhiên 6 Lý thuyết Khoa học tự nhiên 6 SGK KHTN – Kết nối tri thức SGK KHTN – Chân trời sáng tạo SGK KHTN – Cánh Diều SBT KHTN – Kết nối tri thức SBT KHTN – Chân trời sáng tạo SBT KHTN – Cánh Diều Xem thêmMôn Lịch sử và Địa lí Lớp 6SGK Lịch sử và Địa lí – KNTT SGK Lịch sử và Địa lí – CTST SGK Lịch sử và Địa lí – Cánh Diều SBT Lịch sử và Địa lí – KNTT SBT Lịch sử và Địa lí – CTST SBT Lịch sử và Địa lí – Cánh diều Đề thi, kiểm tra Lịch sử và Địa lí – Kết nối tri thức Đề thi, kiểm tra Lịch sử và Địa lí – Cánh Diều Đề thi, kiểm tra Lịch sử và Địa lí – Chân trời sáng tạoMôn Mỹ thuật Lớp 6Mĩ thuật – Kết nối tri thức Mĩ thuật – Chân trời sáng tạo Mĩ thuật – Cánh diều
HỌC NGAY
Môn Toán học Lớp 6Đề thi, đề kiểm tra Toán – Kết nối tri thức Đề thi, đề kiểm tra Toán – Chân trời sáng tạo Đề thi, đề kiểm tra Toán – Cánh diều Vở thực hành Toán 6 SGK Toán – Kết nối tri thức SGK Toán – Chân trời sáng tạo SGK Toán – Cánh diều SBT Toán – Kết nối tri thức SBT Toán – Chân trời sáng tạo Xem thêmMôn Ngữ văn Lớp 6Vở thực hành văn Ôn tập hè Văn lớp 6 Bài tập trắc nghiệm Văn – Cánh diều Bài tập trắc nghiệm Văn – Chân trời sáng tạo Đề thi, đề kiểm tra Văn – Kết nối tri thức Đề thi, đề kiểm tra Văn – Cánh diều Đề thi, đề kiểm tra Văn – Chân trời sáng tạo Soạn văn siêu ngắn – KNTT Văn mẫu 6- Kết nối tri thức Xem thêmMôn Tiếng Anh Lớp 6Bài tập trắc nghiệm Tiếng Anh 6 – English Discovery Đề thi, đề kiểm tra Tiếng Anh – Global Success Đề thi, đề kiểm tra Tiếng Anh – Friends Plus Đề thi, đề kiểm tra Tiếng Anh – iLearn Smart World Đề thi, đề kiểm tra Tiếng Anh – Right on! Đề thi, đề kiểm tra Tiếng Anh – English Discovery Ôn tập hè Tiếng Anh lớp 6 Bài tập trắc nghiệm Tiếng Anh – Global Success Bài tập trắc nghiệm Tiếng Anh – Friends Plus Xem thêmMôn GDCD Lớp 6SGK GDCD – CTST SGK GDCD – Cánh Diều SBT GDCD – Kết nối tri thức SBT GDCD – Chân trời sáng tạo SBT GDCD – Cánh diều SGK GDCD – KNTTMôn Công nghệ Lớp 6Công nghệ – Kết nối tri thức Công nghệ – Cánh Diều Công nghệ – Chân trời sáng tạo SBT Công nghệ – Kết nối tri thức SBT Công nghệ – Cánh diều SBT Công nghệ – Chân trời sáng tạoMôn Tin học Lớp 6Tin học – Kết nối tri thức + chân trời sáng tạo Tin học – Cánh Diều SBT Tin học – Kết nối tri thức SBT Tin học – Cánh DiềuMôn HĐ trải nghiệm, hướng nghiệp Lớp 6SGK Trải nghiệm, hướng nghiệp – Kết nối tri thức SGK Trải nghiệm, hướng nghiệp – Chân trời sáng tạo SGK Trải nghiệm, hướng nghiệp – Cánh diều SBT Trải nghiệm, hướng nghiệp – Kết nối tri thức SBT Trải nghiệm, hướng nghiệp – Chân trời sáng tạo Thực hành Trải nghiệm, hướng nghiệp – Cánh diềuMôn Khoa học tự nhiên Lớp 6Đề thi, đề kiểm tra KHTN – Cánh diều Vở thực hành Khoa học tự nhiên 6 Lý thuyết Khoa học tự nhiên 6 SGK KHTN – Kết nối tri thức SGK KHTN – Chân trời sáng tạo SGK KHTN – Cánh Diều SBT KHTN – Kết nối tri thức SBT KHTN – Chân trời sáng tạo SBT KHTN – Cánh Diều Xem thêmMôn Lịch sử và Địa lí Lớp 6SGK Lịch sử và Địa lí – KNTT SGK Lịch sử và Địa lí – CTST SGK Lịch sử và Địa lí – Cánh Diều SBT Lịch sử và Địa lí – KNTT SBT Lịch sử và Địa lí – CTST SBT Lịch sử và Địa lí – Cánh diều Đề thi, kiểm tra Lịch sử và Địa lí – Kết nối tri thức Đề thi, kiểm tra Lịch sử và Địa lí – Cánh Diều Đề thi, kiểm tra Lịch sử và Địa lí – Chân trời sáng tạoMôn Mỹ thuật Lớp 6Mĩ thuật – Kết nối tri thức Mĩ thuật – Chân trời sáng tạo Mĩ thuật – Cánh diều HỌC NGAY
Môn Toán học Lớp 5SGK Toán – Kết nối tri thức SGK Toán – Chân trời sáng tạo SGK Toán – Cánh diều SGK Toán 5 – Bình Minh SGK Toán lớp 5 VNEN Toán lớp 5 Vở bài tập Toán 5 Bài tập cuối tuần Toán 5 Cùng em học toán lớp 5 Xem thêmMôn Tiếng Anh Lớp 5SGK Tiếng Anh lớp 5 Mới Đề thi vào lớp 6 môn Tiếng Anh Chứng chỉ Cambridge Pre A1 Starters SBT Tiếng Anh lớp 5 Đề thi, đề kiểm tra Tiếng Anh lớp 5 Tiếng Anh – Global Success Tiếng Anh – Family and Friends Tiếng Anh – iLearn Smart Start Tiếng Anh – Explore Our WorldMôn Lịch sử và Địa lí Lớp 5SGK Lịch sử và Địa lí lớp 5 Vở bài tập Lịch sử lớp 5 Vở bài tập Địa lí lớp 5
HỌC NGAY
Môn Toán học Lớp 5SGK Toán – Kết nối tri thức SGK Toán – Chân trời sáng tạo SGK Toán – Cánh diều SGK Toán 5 – Bình Minh SGK Toán lớp 5 VNEN Toán lớp 5 Vở bài tập Toán 5 Bài tập cuối tuần Toán 5 Cùng em học toán lớp 5 Xem thêmMôn Tiếng Anh Lớp 5SGK Tiếng Anh lớp 5 Mới Đề thi vào lớp 6 môn Tiếng Anh Chứng chỉ Cambridge Pre A1 Starters SBT Tiếng Anh lớp 5 Đề thi, đề kiểm tra Tiếng Anh lớp 5 Tiếng Anh – Global Success Tiếng Anh – Family and Friends Tiếng Anh – iLearn Smart Start Tiếng Anh – Explore Our WorldMôn Lịch sử và Địa lí Lớp 5SGK Lịch sử và Địa lí lớp 5 Vở bài tập Lịch sử lớp 5 Vở bài tập Địa lí lớp 5 HỌC NGAY
Môn Toán học Lớp 4Đề thi, đề kiểm tra Toán – Kết nối tri thức Đề thi, đề kiểm tra Toán – Cánh diều Đề thi, đề kiểm tra Toán – Chân trời sáng tạo Toán nâng cao lớp 4 Bài tập trắc nghiệm Toán – Kết nối tri thức SGK Toán – Kết nối tri thức Bài tập trắc nghiệm Toán – Cánh diều SGK Toán – Chân trời sáng tạo Bài tập trắc nghiệm Toán – Chân trời sáng tạo Xem thêmMôn Tiếng Anh Lớp 4Bài tập trắc nghiệm Tiếng Anh – Family and Friends Bài tập trắc nghiệm Tiếng Anh – iLearn Smart Start Đề thi, đề kiểm tra Tiếng Anh – Global Success Đề thi, đề kiểm tra Tiếng Anh – Family and Friends Đề thi, đề kiểm tra Tiếng Anh – iLearn Smart Start Tiếng Anh – Global Sucess Đề thi, đề kiểm tra Tiếng Anh – Phonics Smart Tiếng Anh – Family and Friends Đề thi, đề kiểm tra Tiếng Anh – Explore Our World Xem thêmMôn Công nghệ Lớp 4SGK Công nghệ – Kết nối tri thức SGK Công nghệ – Chân trời sáng tạo SGK Công nghệ – Cánh diềuMôn HĐ trải nghiệm, hướng nghiệp Lớp 4SGK Hoạt động trải nghiệm – Kết nối tri thức SGK Hoạt động trải nghiệm – Cánh diều SGK Hoạt động trải nghiệm – Chân trời sáng tạo Bản 1 SGK Hoạt động trải nghiệm – Chân trời sáng tạo Bản 2Môn Giáo dục thể chất Lớp 4SGK Giáo dục thể chất – Kết nối tri thức SGK Giáo dục thể chất – Cánh diều SGK Giáo dục thể chất – Chân trời sáng tạoMôn Lịch sử và Địa lí Lớp 4SGK Lịch sử và Địa lí – Kết nối tri thức SGK Lịch sử và Địa lí – Chân trời sáng tạo SGK Lịch sử và Địa lí – Cánh diềuMôn Âm nhạc Lớp 4SGK Âm nhạc – Kết nối tri thức SGK Âm nhạc – Chân trời sáng tạo SGK Âm nhạc – Cánh diềuMôn Mỹ thuật Lớp 4SGK Mĩ thuật – Kết nối tri thức SGK Mĩ thuật – Cánh diều SGK Mĩ thuật – Chân trời sáng tạo bản 1 SGK Mĩ thuật – Chân trời sáng tạo bản 2Môn Tiếng việt Lớp 4Đề thi, đề kiểm tra Tiếng Việt – Kết nối tri thức Đề thi, đề kiểm tra Tiếng Việt – Chân trời sáng tạo Đề thi, đề kiểm tra Tiếng Việt – Cánh diều Tiếng Việt – Kết nối tri thức Tiếng Việt – Chân trời sáng tạo Tiếng Việt – Cánh diều VBT Tiếng Việt – Kết nối tri thức SGK Tiếng Việt 4 Cùng em học Tiếng Việt 4 Xem thêm
HỌC NGAY
Môn Toán học Lớp 4Đề thi, đề kiểm tra Toán – Kết nối tri thức Đề thi, đề kiểm tra Toán – Cánh diều Đề thi, đề kiểm tra Toán – Chân trời sáng tạo Toán nâng cao lớp 4 Bài tập trắc nghiệm Toán – Kết nối tri thức SGK Toán – Kết nối tri thức Bài tập trắc nghiệm Toán – Cánh diều SGK Toán – Chân trời sáng tạo Bài tập trắc nghiệm Toán – Chân trời sáng tạo Xem thêmMôn Tiếng Anh Lớp 4Bài tập trắc nghiệm Tiếng Anh – Family and Friends Bài tập trắc nghiệm Tiếng Anh – iLearn Smart Start Đề thi, đề kiểm tra Tiếng Anh – Global Success Đề thi, đề kiểm tra Tiếng Anh – Family and Friends Đề thi, đề kiểm tra Tiếng Anh – iLearn Smart Start Tiếng Anh – Global Sucess Đề thi, đề kiểm tra Tiếng Anh – Phonics Smart Tiếng Anh – Family and Friends Đề thi, đề kiểm tra Tiếng Anh – Explore Our World Xem thêmMôn Công nghệ Lớp 4SGK Công nghệ – Kết nối tri thức SGK Công nghệ – Chân trời sáng tạo SGK Công nghệ – Cánh diềuMôn HĐ trải nghiệm, hướng nghiệp Lớp 4SGK Hoạt động trải nghiệm – Kết nối tri thức SGK Hoạt động trải nghiệm – Cánh diều SGK Hoạt động trải nghiệm – Chân trời sáng tạo Bản 1 SGK Hoạt động trải nghiệm – Chân trời sáng tạo Bản 2Môn Giáo dục thể chất Lớp 4SGK Giáo dục thể chất – Kết nối tri thức SGK Giáo dục thể chất – Cánh diều SGK Giáo dục thể chất – Chân trời sáng tạoMôn Lịch sử và Địa lí Lớp 4SGK Lịch sử và Địa lí – Kết nối tri thức SGK Lịch sử và Địa lí – Chân trời sáng tạo SGK Lịch sử và Địa lí – Cánh diềuMôn Âm nhạc Lớp 4SGK Âm nhạc – Kết nối tri thức SGK Âm nhạc – Chân trời sáng tạo SGK Âm nhạc – Cánh diềuMôn Mỹ thuật Lớp 4SGK Mĩ thuật – Kết nối tri thức SGK Mĩ thuật – Cánh diều SGK Mĩ thuật – Chân trời sáng tạo bản 1 SGK Mĩ thuật – Chân trời sáng tạo bản 2Môn Tiếng việt Lớp 4Đề thi, đề kiểm tra Tiếng Việt – Kết nối tri thức Đề thi, đề kiểm tra Tiếng Việt – Chân trời sáng tạo Đề thi, đề kiểm tra Tiếng Việt – Cánh diều Tiếng Việt – Kết nối tri thức Tiếng Việt – Chân trời sáng tạo Tiếng Việt – Cánh diều VBT Tiếng Việt – Kết nối tri thức SGK Tiếng Việt 4 Cùng em học Tiếng Việt 4 Xem thêm HỌC NGAY
Môn Toán học Lớp 3Bài tập trắc nghiệm Toán – Cánh diều Ôn tập hè Toán – Kết nối tri thức Ôn tập hè Toán – Cánh diều Ôn tập hè Toán – Chân trời sáng tạo Đề thi, đề kiểm tra Toán – Kết nối tri thức Bài tập cuối tuần môn Toán 3 Đề thi, đề kiểm tra Toán – Chân trời sáng tạo Đề thi, đề kiểm tra Toán – Cánh diều Cùng em học Toán 3 Xem thêmMôn Tiếng Anh Lớp 3Bài tập trắc nghiệm Tiếng Anh – iLearn Smart Start Đề thi, đề kiểm tra Tiếng Anh – Global Success Đề thi, đề kiểm tra Tiếng Anh – Family and Friends Đề thi, đề kiểm tra Tiếng Anh – Explore Our World Đề thi, đề kiểm tra Tiếng Anh – iLearn Smart Start Đề thi, đề kiểm tra Tiếng Anh – Phonics Smart Chứng chỉ Cambridge Pre A1 Starters Tiếng Anh – Global Success Tiếng Anh – Family and Friends Xem thêmMôn Tin học Lớp 3SGK Tin học – Kết nối tri thức SGK Tin học – Chân trời sáng tạo SGK Tin học – Cánh diềuMôn HĐ trải nghiệm, hướng nghiệp Lớp 3SGK Hoạt động trải nghiệm- Kết nối tri thức SGK Hoạt động trải nghiệm- Chân trời sáng tạo SGK Hoạt động trải nghiệm – Cánh diềuMôn Tiếng việt Lớp 3Tiếng Việt – Kết nối tri thức Tiếng Việt – Chân trời sáng tạo Tiếng Việt – Cánh diều VBT Tiếng Việt – Kết nối tri thức VBT Tiếng Việt – Chân trời sáng tạo VBT Tiếng Việt – Cánh diều Văn mẫu – Kết nối tri thức Cùng em học Tiếng Việt 3 Văn mẫu lớp 3Môn Tự nhiên và xã hội Lớp 3Tự nhiên và xã hội – Kết nối tri thức Tự nhiên và xã hội – Chân trời sáng tạo Tự nhiên và xã hội – Cánh diều
HỌC NGAY
Môn Toán học Lớp 3Bài tập trắc nghiệm Toán – Cánh diều Ôn tập hè Toán – Kết nối tri thức Ôn tập hè Toán – Cánh diều Ôn tập hè Toán – Chân trời sáng tạo Đề thi, đề kiểm tra Toán – Kết nối tri thức Bài tập cuối tuần môn Toán 3 Đề thi, đề kiểm tra Toán – Chân trời sáng tạo Đề thi, đề kiểm tra Toán – Cánh diều Cùng em học Toán 3 Xem thêmMôn Tiếng Anh Lớp 3Bài tập trắc nghiệm Tiếng Anh – iLearn Smart Start Đề thi, đề kiểm tra Tiếng Anh – Global Success Đề thi, đề kiểm tra Tiếng Anh – Family and Friends Đề thi, đề kiểm tra Tiếng Anh – Explore Our World Đề thi, đề kiểm tra Tiếng Anh – iLearn Smart Start Đề thi, đề kiểm tra Tiếng Anh – Phonics Smart Chứng chỉ Cambridge Pre A1 Starters Tiếng Anh – Global Success Tiếng Anh – Family and Friends Xem thêmMôn Tin học Lớp 3SGK Tin học – Kết nối tri thức SGK Tin học – Chân trời sáng tạo SGK Tin học – Cánh diềuMôn HĐ trải nghiệm, hướng nghiệp Lớp 3SGK Hoạt động trải nghiệm- Kết nối tri thức SGK Hoạt động trải nghiệm- Chân trời sáng tạo SGK Hoạt động trải nghiệm – Cánh diềuMôn Tiếng việt Lớp 3Tiếng Việt – Kết nối tri thức Tiếng Việt – Chân trời sáng tạo Tiếng Việt – Cánh diều VBT Tiếng Việt – Kết nối tri thức VBT Tiếng Việt – Chân trời sáng tạo VBT Tiếng Việt – Cánh diều Văn mẫu – Kết nối tri thức Cùng em học Tiếng Việt 3 Văn mẫu lớp 3Môn Tự nhiên và xã hội Lớp 3Tự nhiên và xã hội – Kết nối tri thức Tự nhiên và xã hội – Chân trời sáng tạo Tự nhiên và xã hội – Cánh diều HỌC NGAY
Môn Toán học Lớp 2Bài tập trắc nghiệm Toán – Chân trời sáng tạo Bài tập trắc nghiệm Toán – Cánh diều SGK Toán – Kết nối tri thức SGK Toán – Chân trời sáng tạo SGK Toán – Cánh Diều VBT Toán – KNTT VBT Toán – CTST Đề thi, đề kiểm tra Toán – Kết nối tri thức Đề thi, đề kiểm tra Toán – Chân trời sáng tạo Xem thêmMôn Tiếng Anh Lớp 2SBT English Discovery SBT Explore Our World Đề thi, đề kiểm tra Tiếng Anh – Global Success Đề thi, đề kiểm tra Tiếng Anh – Family and Friends Đề thi, đề kiểm tra Tiếng Anh – iLearn Smart Start Đề thi, đề kiểm tra Tiếng Anh – Phonics Smart Đề thi, đề kiểm tra Tiếng Anh – English Discovery Chứng chỉ Cambridge Pre A1 Starters SBT Kết nối tri thức Xem thêmMôn HĐ trải nghiệm, hướng nghiệp Lớp 2VBT Hoạt động trải nghiệm – Chân trời sáng tạo VTH Hoạt động trải nghiệm – Cánh Diều VBT Hoạt động trải nghiệm – Kết nối tri thứcMôn Âm nhạc Lớp 2Âm nhạc 2 – Kết nối tri thức Âm nhạc 2 – Chân trời sáng tạo Âm nhạc 2 – Cánh diều VBT Âm nhạc – Kết nối tri thức VBT Âm nhạc – Chân trời sáng tạo VBT Âm nhạc – Cánh diềuMôn Tiếng việt Lớp 2Tiếng Việt – Kết nối tri thức Tiếng Việt – Chân trời sáng tạo Tiếng Việt – Cánh Diều Văn mẫu – Kết nối tri thức Văn mẫu – Chân trời sáng tạo Văn mẫu – Cánh diều VBT Tiếng Việt – Kết nối tri thức VBT Tiếng Việt – Chân trời sáng tạo VBT Tiếng Việt – Cánh diều Xem thêm
HỌC NGAY
Môn Toán học Lớp 2Bài tập trắc nghiệm Toán – Chân trời sáng tạo Bài tập trắc nghiệm Toán – Cánh diều SGK Toán – Kết nối tri thức SGK Toán – Chân trời sáng tạo SGK Toán – Cánh Diều VBT Toán – KNTT VBT Toán – CTST Đề thi, đề kiểm tra Toán – Kết nối tri thức Đề thi, đề kiểm tra Toán – Chân trời sáng tạo Xem thêmMôn Tiếng Anh Lớp 2SBT English Discovery SBT Explore Our World Đề thi, đề kiểm tra Tiếng Anh – Global Success Đề thi, đề kiểm tra Tiếng Anh – Family and Friends Đề thi, đề kiểm tra Tiếng Anh – iLearn Smart Start Đề thi, đề kiểm tra Tiếng Anh – Phonics Smart Đề thi, đề kiểm tra Tiếng Anh – English Discovery Chứng chỉ Cambridge Pre A1 Starters SBT Kết nối tri thức Xem thêmMôn HĐ trải nghiệm, hướng nghiệp Lớp 2VBT Hoạt động trải nghiệm – Chân trời sáng tạo VTH Hoạt động trải nghiệm – Cánh Diều VBT Hoạt động trải nghiệm – Kết nối tri thứcMôn Âm nhạc Lớp 2Âm nhạc 2 – Kết nối tri thức Âm nhạc 2 – Chân trời sáng tạo Âm nhạc 2 – Cánh diều VBT Âm nhạc – Kết nối tri thức VBT Âm nhạc – Chân trời sáng tạo VBT Âm nhạc – Cánh diềuMôn Tiếng việt Lớp 2Tiếng Việt – Kết nối tri thức Tiếng Việt – Chân trời sáng tạo Tiếng Việt – Cánh Diều Văn mẫu – Kết nối tri thức Văn mẫu – Chân trời sáng tạo Văn mẫu – Cánh diều VBT Tiếng Việt – Kết nối tri thức VBT Tiếng Việt – Chân trời sáng tạo VBT Tiếng Việt – Cánh diều Xem thêm HỌC NGAY
Môn Tiếng Anh Lớp 1Chứng chỉ Cambridge Pre A1 StartersMôn Tiếng việt Lớp 1Đề thi, đề kiểm tra Tiếng Việt 1 SGK Tiếng Việt – Kết nối tri thức SGK Tiếng Việt – Chân trời sáng tạo SGK Tiếng Việt – Cánh diềuMôn Đạo đức Lớp 1VBT Đạo Đức 1
HỌC NGAY
Môn Tiếng Anh Lớp 1Chứng chỉ Cambridge Pre A1 StartersMôn Tiếng việt Lớp 1Đề thi, đề kiểm tra Tiếng Việt 1 SGK Tiếng Việt – Kết nối tri thức SGK Tiếng Việt – Chân trời sáng tạo SGK Tiếng Việt – Cánh diềuMôn Đạo đức Lớp 1VBT Đạo Đức 1


















